Если у вас или вашего близкого диагностировали рак костей, чем больше информации о заболевании вы получите, тем легче будет справиться с тревогой и принять правильное решение о выборе методов лечения и реабилитации. Для пациентов столкнувшихся с раком и их родственников мы перевели статьи с сайта Американского сообщества онкологических пациентов https://www.cancer.org/cancer/types/bone-cancer.html
Данная информация посвящена раку костей, наиболее часто встречающемуся у взрослых и возникающему в костях (первичный рак костей).
Рак костей — это опухоли, которые начинают развиваться в кости. Это не то же самое, что метастазы в кости, которые возникают, когда рак начинается в другой части тела, а затем распространяется на кости. Раковые заболевания крови, такие как лейкемия, также не считаются раком костей, хотя они могут обнаруживаться внутри костей, где живут клетки, образующие кровь.
Рак костей — это разновидность саркомы. Саркома — это рак, который развивается, когда клетки, которые обычно составляют соединительную ткань организма, начинают бесконтрольно размножаться. К соединительной ткани относятся кости и хрящи, а также мышцы, жировая ткань, выстилка суставов и кровеносных сосудов.
Кости состоят из множества типов клеток и тканей. Изначально это были стволовые клетки, которые со временем превращаются в специализированные клетки, формирующие и поддерживающие соединительную ткань вашего тела. Большинство из них могут перерасти в рак, в том числе:
- Остеобласты: клетки, которые образуют новую костную ткань.
- Остеокласты: клетки, которые растворяют старую костную ткань.
- Остеоциты: клетки, поддерживающие костную ткань.
- Фибробласты: клетки, которые образуют волокнистые ткани, такие как связки и сухожилия.
- Фиброциты: клетки, поддерживающие фиброзную ткань.
- Хондробласты: клетки, которые строят новый хрящ и коллаген.
- Хондроциты: клетки, составляющие хрящевую ткань.
Статистические данные
Первичные опухоли костей встречаются редко. Чаще рак распространяется на кости (метастазы в кости), чем рак возникает в костях (первичный рак костей).
По оценкам Американского онкологического общества, в 2026 году ожидается следующее количество случаев первичного рака костей и суставов:
- Выявлено около 4110 новых случаев заболевания (2290 у мужчин и 1820 у женщин).
- Около 2210 смертей (1240 среди мужчин и 970 среди женщин).
Это включает в себя онкологические заболевания как у детей, так и у взрослых.
Первичные опухоли костей (рак, начинающийся в костях) встречаются редко, составляя менее 1% от всех случаев рака. У взрослых рак, распространяющийся на кости из других органов (известный как метастазы в кости ), встречается гораздо чаще, чем первичные опухоли костей.
Какие виды рака костей встречаются чаще всего?
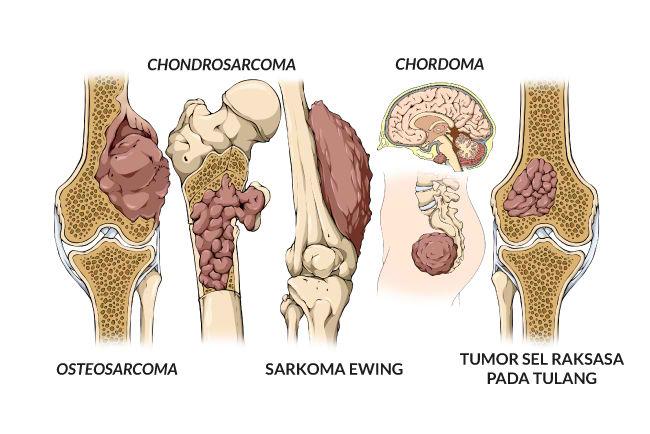
Остеосаркома является наиболее распространенным типом первичного рака костей в целом, за ней следуют хондросаркома и саркома Юинга. Однако это варьируется в зависимости от возрастной группы.
У взрослых наиболее распространенным первичным раком костей является хондросаркома. За ней следуют остеосаркомы, хордомы и недифференцированные плеоморфные саркомы. Другие виды рака костей встречаются гораздо реже.
У детей и подростков наиболее распространенными видами рака костей являются остеосаркома и саркома Юинга.
Прогноз для людей с раком костей зависит от многих факторов, включая тип рака костей, локализацию опухоли, наличие метастазов на момент обнаружения, возраст и общее состояние здоровья пациента, а также эффективность лечения.
Виды рака костей
Виды первичных раковых заболеваний костей
Термин «первичный рак кости» относится к любому раку, который начинается в кости. Существует множество видов первичного рака костей. Их часто называют в зависимости от типа клеток, которые в них обнаруживаются. Например, хондросаркома состоит из аномальных хондроцитов, похожих на хрящевую ткань.
Для вас и вашей лечащей команды важно знать, из каких типов клеток состоит ваш рак кости. Это даст больше информации о возможном росте рака и о том, как он может реагировать на определенные методы лечения.
Остеосаркома. Остеосаркома — наиболее распространенный первичный рак костей. Она начинается на ранней стадии развития костных клеток. Этот тип рака чаще всего встречается у молодых людей в возрасте от 10 до 30 лет, но примерно у 1 из 5 остеосарком развивается у людей старше 60 лет. У людей среднего возраста он встречается редко. Также он чаще встречается у мужчин, чем у женщин. Эти опухоли часто обнаруживаются в костях рук, ног или таза.
Хондросаркома. Хондросаркома начинается на ранних стадиях развития хрящевых клеток. Это второй по распространенности первичный рак костей. У людей моложе 20 лет она встречается редко, а риск развития заболевания возрастает с возрастом. Хондросаркомы могут возникать в любом месте тела, где есть хрящевая ткань. Чаще всего они появляются в костях таза (тазобедренного сустава), ног или рук.
Хондросаркомы классифицируются по степени злокачественности от I (1) до III (3). Это показатель того, насколько быстро рак, вероятно, будет расти, исходя из того, как выглядят клетки под микроскопом. Чем ниже степень злокачественности, тем медленнее рак, как правило, растет и тем меньше вероятность его распространения:
- Низкодифференцированные хондросаркомы (I степени) обычно растут медленнее всего и крайне маловероятно распространяются. Их также называют атипичными хрящевыми опухолями (АКТ) .
- Хондросаркомы средней степени злокачественности (II степень) имеют несколько более высокую вероятность распространения.
- Высокозлокачественные хондросаркомы (III степени) наиболее склонны к метастазированию.
Большинство хондросарком относятся к I или II степени злокачественности.
Помимо степени злокачественности, типичные хондросаркомы могут также называться в зависимости от места их произрастания.
- Центральная хондросаркома развивается внутри кости, где находится костный мозг.
- Вторичная периферическая хондросаркома развивается в хрящевой оболочке существующей остеохондромы, одной из наиболее распространенных доброкачественных опухолей костей.
- Периостальная хондросаркома развивается на поверхности кости.
Хондросаркомы, растущие в центре кости, являются наиболее распространенными.
Редкие подтипы хондросаркомы. Небольшое количество хондросаркомы имеет характерные признаки, которые можно увидеть под микроскопом. Эти редкие подтипы часто имеют другой прогноз (исход заболевания).
- Дедифференцированные хондросаркомы изначально представляют собой типичные хондросаркомы, но затем некоторые участки опухоли трансформируются в клетки, подобные клеткам высокозлокачественной саркомы, такой как остеосаркома, фибросаркома или высокозлокачественная недифференцированная плеоморфная саркома. Этот тип хондросаркомы, как правило, развивается у пожилых людей и растет быстрее, чем большинство других хондросарком.
- Мезенхимальные хондросаркомы, как правило, развиваются у молодых взрослых. Они часто быстро растут и с большей вероятностью рецидивируют после лечения.
- Светлоклеточные хондросаркомы встречаются редко. Они, как правило, растут медленно и могут рецидивировать спустя много лет после лечения. Чаще встречаются у мужчин.
Доброкачественные опухоли в хряще. Доброкачественные (не раковые) опухоли, такие как энхондромы и остеохондромы, чаще встречаются в хрящевой ткани, чем хондросаркомы. Эти доброкачественные опухоли редко перерождаются в рак. У людей с большим количеством таких опухолей несколько выше вероятность развития рака, но это нечастое явление.
Саркома Юинга (опухоль Юинга). Саркома Юинга — третий по распространенности тип рака костей в целом и второй по распространенности тип первичного рака костей у детей, подростков и молодых взрослых. Эти опухоли редко встречаются у взрослых старше 30 лет.
Большинство опухолей Юинга развиваются в костях, но могут возникать и в других тканях и органах. Наиболее распространенными местами локализации этого рака являются тазовые кости, кости грудной клетки (например, ребра или лопатки), кости позвоночника и длинные кости ног.
Недифференцированные мелкоклеточные саркомы (подобные саркоме Юинга). Под микроскопом эти опухоли похожи на саркому Юинга, но отличаются уникальными генетическими изменениями.
Изменения гена BCOR: опухоли с изменениями в гене BCOR чаще встречаются у мужчин, и большинство из них — у детей. Опухоли с такими изменениями в гене обнаруживаются в области таза и длинных костей рук и ног.
Изменения гена CIC: опухоли с изменениями в гене CIC чаще встречаются у мужчин и молодых людей в возрасте от 20 до 40 лет. Эти опухоли чаще растут в мягких тканях, чем в костях.
Слияния генов EWSR1, помимо EWSR1: слияния ETS, наблюдаемые при саркоме Юинга. Опухоли с не-Ewing- генными слияниями EWSR1 чаще встречаются у мужчин и пожилых людей. Эти опухоли могут иметь различные характеристики в зависимости от того, какое именно изменение гена в них происходит.
Высокозлокачественная недифференцированная плеоморфная саркома (НПС) кости. Ранее этот вид рака был известен как злокачественная фиброзная гистиоцитома (ЗФГ) кости . Чаще всего он поражает мягкие ткани, такие как жировая ткань или мышцы, но может также затрагивать кости. Чаще всего он поражает кости рук или ног (часто в области коленей). Этот вид рака чаще всего встречается у пожилых и людей среднего возраста.
Фибросаркома кости. Фибросаркома — это ещё один вид рака, который чаще развивается в мягких тканях, чем в костях. Обычно она встречается у людей среднего возраста. Чаще всего поражаются кости ног.
Гигантоклеточная опухоль кости. Этот тип первичной опухоли кости может быть как доброкачественным (не раковым), так и злокачественным. Доброкачественная форма встречается чаще. Такие опухоли чаще всего встречаются у людей в возрасте 20–30 лет. Гигантоклеточные опухоли костей обычно поражают руки или ноги (как правило, около колен). Они редко распространяются на отдаленные части тела, но после операции могут рецидивировать в месте своего возникновения, причем неоднократно. С каждым рецидивом вероятность распространения опухоли на другие части тела, чаще всего на легкие, немного возрастает.
Хордома. Этот редкий тип опухоли кости встречается в костях позвоночника, чаще всего в основании позвоночника (крестце) или у основания черепа. Чаще всего он развивается у пожилых людей. Может развиваться и у детей, но это случается редко. Хордомы растут медленно и могут иметь нечеткие симптомы, что затрудняет диагностику. Эти опухоли, как правило, рецидивируют вблизи первоначального очага и иногда могут распространяться на другие части тела, такие как легкие или печень.
Доброкачественные (не раковые) опухоли костей
Не все опухоли костей являются раком. Доброкачественные опухоли костей не распространяются на другие части тела. Обычно они не представляют угрозы для жизни, и часто их можно полностью удалить хирургическим путем. Существует множество типов доброкачественных опухолей костей, в том числе:
- Остеоидная остеома
- Остеобластома
- Остеохондрома
- Хондробластома
- Хондромиксоидная фиброма
- Энхондрома
- Неоссифицирующая фиброма
- Аневризматическая костная киста
- Однокамерная костная киста
- Эозинофильная гранулема кости
- Доброкачественная гигантоклеточная опухоль кости
Факторы риска и что вызывает рак костей
Точная причина большинства опухолей костей неизвестна. Ученые выявили некоторые генетические и экологические факторы риска, но у большинства людей с раком костей нет известных факторов риска. Фактор риска — это любой фактор, влияющий на вероятность развития у человека такого заболевания, как рак.
Что вызывает рак костей?
Исследователи выявили некоторые факторы, повышающие риск развития рака костей. Однако, по большей части, до конца не ясно, как именно эти факторы риска могут вызывать развитие рака костей. Продолжаются исследования для выяснения этих деталей.
Известно, что специфические изменения генов (мутации) в нормальных клетках костной ткани, хрящевых клетках и других клетках опорно-двигательного аппарата чаще встречаются при некоторых типах рака костей. Эти изменения происходят в генах, контролирующих рост клеток или восстанавливающих поврежденную ДНК . Это может привести к образованию раковых клеток в этих клетках.тНекоторые факторы окружающей среды также могут повышать риск развития рака костей.
Генетические факторы риска рака костей.
Большинство изменений в генах (мутаций), вызывающих рак костей, происходят в течение жизни человека. Они называются приобретенными мутациями . Лишь небольшое число людей наследуют от родителей генные мутации , повышающие риск развития рака костей.
Наследственные генные мутации в зависимости от типа рака
Исследователи обнаружили наследственные генные мутации, повышающие риск развития некоторых видов рака костей.
Остеосаркома. Существует ряд наследственных изменений генов, которые могут повысить риск развития остеосаркомы. К ним относятся такие заболевания, как синдром Ли-Фраумени, наследственная ретинобластома, синдром Ротмунда-Томсона и другие генетические расстройства.
Хондросаркома. Наследственные множественные остеохондромы (множественные наследственные экзостозы). Это заболевание часто вызывается наследственным изменением гена-супрессора опухолей, называемого EXT1 или EXT2 . При этом состоянии происходит рост множественных остеохондром на костях тела. Остеохондромы являются доброкачественными образованиями (не раком), но примерно в 5% случаев остеохондромы трансформируются в хондросаркому.
Болезнь Оллиера/синдром Маффуччи.
Эти заболевания вызваны изменениями в генах IDH1 или IDH2 .
- Болезнь Олье характеризуется ростом энхондром, доброкачественных опухолей хряща.
- Синдром Маффуччи характеризуется ростом энхондром и гемангиом (доброкачественных опухолей кровеносных сосудов).
Примерно у 50% людей с этими редкими заболеваниями в течение жизни энхондрома трансформируется в хондросаркому.
Саркома Юинга. Исследователи пока не обнаружили наследственных изменений генов, повышающих риск развития саркомы Юинга.
Недифференцированные мелкоклеточные саркомы (подобные саркоме Юинга). Исследователи пока не обнаружили наследственных изменений генов, повышающих риск развития этих редких опухолей.
Фибросаркома кости. Исследователи пока не обнаружили наследственных изменений генов, повышающих риск развития этой редкой опухоли.
Гигантоклеточная опухоль кости. Гигантоклеточные опухоли были обнаружены у людей с синдромом Нунан , генетическим заболеванием, влияющим на рост и развитие. Это заболевание может приводить к тому, что люди будут ниже среднего роста, иметь уникальные черты лица и задержки в развитии, а также проблемы с сердцем, почками и костями.
Хордома. Большинство хордом не имеют известной причины возникновения, но небольшое количество хордом, по-видимому, передается по наследству. Это называется семейной хордомой . Она часто связана с изменением (мутацией) в гене TBXT , который человек наследует от одного из родителей. У людей с туберозным склерозом, по-видимому, высок риск развития хордомы в детском возрасте, хотя в целом это заболевание встречается редко. Туберозный склероз — это наследственный синдром, вызванный дефектом (мутацией) в гене TSC1 или TSC2 .
Другие условия
Ученые также обнаружили, что условия, при которых кости часто растут или перестраиваются, могут повышать риск развития рака костей.
Например, болезнь Педжета — это заболевание, при котором кости быстро перекатываются, что приводит к их ослаблению и увеличению в размерах. Люди с болезнью Педжета могут быть подвержены более высокому риску развития некоторых опухолей костей, таких как остеосаркома или гигантоклеточные опухоли костей. В некоторых случаях болезнь Педжета передается по наследству, но у многих людей причина этого заболевания до конца не изучена.
Факторы экологического риска
Фактор риска окружающей среды — это то, что в вашем окружении повышает риск развития таких заболеваний, как рак. Некоторые факторы риска окружающей среды связаны с раком костей.
Предшествующая лучевая терапия. У людей, прошедших лучевую терапию, обычно для лечения другого вида рака, наблюдается незначительно повышенный риск развития рака костей в области, подвергшейся облучению. Риск выше у людей, проходивших лечение в молодом возрасте, особенно в детстве, и у тех, кто получал более высокие дозы радиации. Эти виды рака, как правило, развиваются спустя много лет после лучевой терапии, часто спустя десятилетия. Чаще всего это остеосаркомы, но иногда встречаются и менее распространенные виды рака костей, такие как фибросаркома кости или недифференцированная плеоморфная саркома кости.
Предшествующая химиотерапия. Лечение алкилирующими химиопрепаратами связано с развитием рака костей, такого как остеосаркома, у людей, ранее получавших лечение этими препаратами от другого вида рака. К алкилирующим химиопрепаратам относятся циклофосфамид, ифосфамид, бусульфан, мелфалан и другие.
Другие факторы риска
Возраст и раса также могут быть факторами риска для некоторых видов рака костей.
Возраст. Некоторые виды опухолей костей могут встречаться чаще или реже в зависимости от возраста. Например:
- Остеосаркома и саркома Юинга чаще встречаются у детей и молодых взрослых.
- Хондросаркомы чаще встречаются у пожилых людей.
Можно ли предотвратить рак костей?
Большинство известных факторов риска развития рака костей изменить невозможно, включая возраст, некоторые заболевания костей и наследственные состояния. Известных причин рака костей, связанных с образом жизни или окружающей средой, кроме предшествующего облучения или химиотерапии, не существует. Поэтому на данный момент нет способов защититься от большинства видов рака костей.
Симптомы рака костей
Опухоли костей могут поражать любые кости в организме. Они также могут поражать смежные ткани, например, хрящ. Симптомы рака костей зависят от местоположения опухоли, ее размера и от того, распространилась ли она на другие части тела.
Симптомы рака костей, вызванные основной опухолью.
Наиболее распространенные симптомы рака костей:
- Боль
- Уплотнение или припухлость
- Переломы
- Снижение веса
- Усталость.
Боль. Боль в области опухоли — наиболее распространенный признак рака кости. Поначалу боль может быть не постоянной. Она может усиливаться ночью или при нагрузке на кость, например, при ходьбе, если опухоль находится в кости ноги. Со временем боль может стать более постоянной и усиливаться при физической активности. Раковые клетки в костях позвоночника могут сдавливать нервы, отходящие от спинного мозга. Это может вызывать онемение, покалывание или слабость в различных частях тела, в зависимости от локализации опухоли. Иногда опухоль ослабляет кость до такой степени, что она ломается, что может вызвать внезапную, сильную боль.
Уплотнение или припухлость. Некоторые опухоли костей вызывают образование шишки или припухлости в этой области, хотя это может произойти лишь спустя некоторое время после того, как в этом месте появится боль. Раковые опухоли в костях шеи иногда вызывают образование уплотнения в задней части горла, что может привести к затруднению глотания или дыхания.
Переломы. Рак костей может ослабить кость, но обычно это не приводит к перелому. Люди с переломом, произошедшим рядом с опухолью кости или проходящим через нее, обычно описывают внезапную, сильную боль в кости, которая болела в течение нескольких месяцев.
Снижение веса. При раке организм расходует гораздо больше энергии, поскольку раковые клетки растут и делятся. Из-за этого у некоторых людей с раком может наблюдаться потеря веса без изменения диеты или физических упражнений.
Усталость. При раке человек может чувствовать себя более уставшим или слабым. Это характерно для многих видов рака, а не только для рака костей. Усталость может быть вызвана множеством причин, помимо рака.
Признаки или симптомы, вызванные метастатическим раком костей.
Если рак костей распространяется на другие органы, он может вызывать и другие симптомы. Например, если рак распространится на легкие, это может привести к кашлю или затруднению дыхания. Рак костей встречается нечасто, и его симптомы чаще всего обусловлены другими заболеваниями, такими как травмы или артрит. Тем не менее, если симптомы сохраняются длительное время или усиливаются, важно обратиться к врачу, чтобы установить причину и при необходимости назначить лечение.
Диагностика рака костей
Диагностика рака костей часто включает в себя физический осмотр, визуальные методы исследования и анализы крови, а также биопсию опухоли для подтверждения диагноза. Если диагноз рака костей подтверждается биопсией, проводятся подробные исследования для получения дополнительной информации о заболевании и определения наилучших методов лечения.
Визуальные методы исследования также используются во время и после лечения, чтобы отслеживать эффективность терапии. Медицинская команда соберет полный анамнез, чтобы узнать больше о симптомах. Они также могут спросить о возможных факторах риска развития рака костей, таких как предыдущие методы лечения рака, например, лучевая терапия, или наличие онкологических заболеваний в семейном анамнезе. Затем медицинская бригада осмотривает, выявляя признаки, указывающие на причину появления симптомов. Во время этого физического осмотра они могут:
- Осмотреть или прощупать аномальное уплотнение или болезненный участок.
- Проверить нормально ли функционирует и двигается пораженный участок, если шишка находится на руке или ноге.
- Обратить внимание на проблемы в других частях тела.
Если у пациента опухоль в кости, важно, чтобы медицинская команда выяснила, возникла ли опухоль именно там (первичная опухоль кости) или распространилась туда из другой части тела.
После медицинского осмотра
После обследования, если медицинская команда заподозрит рак костей или другой тип опухоли костей, они проведут дополнительные анализы. Это может включать в себя:
- Диагностические исследования с помощью методов визуализации
- Биопсии
- Анализы крови
Эти анализы важны, поскольку многие симптомы и признаки рака костей могут быть вызваны травмами, другими заболеваниями, такими как инфекции, или другими видами рака.
Диагностические исследования с помощью методов визуализации
Диагностические исследования с помощью методов визуализации используются для получения изображений внутренних органов. Визуализация может проводиться по ряду причин. Она может помочь медицинской команде:
- Выяснить не является ли подозрительный участок раковой опухолью.
- Определить не возник ли рак в другой части вашего тела.
- Узнайть насколько далеко распространился рак.
- Определить эффективно ли лечение.
- Обратить внимание на возможные признаки рецидива рака после лечения.
Рентгеновский снимок. Рентгеновское исследование часто является первым методом диагностики, если врачи подозревают опухоль кости. Они часто могут распознать опухоль по рентгеновским снимкам кости. Опухоли могут иметь «неровные» края вместо того, чтобы выглядеть сплошными на рентгеновском снимке, или они могут выглядеть как отверстие в кости. Иногда врачи могут увидеть опухоль, которая может распространяться на близлежащие ткани, такие как мышцы или жировая ткань.
На рентгеновском снимке у вашей медицинской команды может возникнуть сильное подозрение, что обнаруженная аномалия является раком кости, но для точной диагностики обычно требуется биопсия. Рентген грудной клетки. Рентгеновские снимки также можно использовать для определения распространения рака на легкие. Рентген позволяет обнаружить более крупные опухоли, но он уступает компьютерной томографии (КТ) в выявлении мелких опухолей. Если вам сделают КТ грудной клетки, рентгеновский снимок может и не понадобиться.
Магнитно-резонансная томография (МРТ). МРТ позволяет получить детальные изображения мягких тканей внутри тела. Для этого используются радиоволны и мощные магниты вместо рентгеновских лучей, поэтому радиация отсутствует. Перед сканированием в вену может быть введен контрастный препарат гадолиний для лучшего отображения деталей. МРТ обычно показывает более детальные изображения, чем КТ. МРТ для исследования патологического участка: Если врачи обнаруживают на рентгеновском снимке патологический участок кости, они часто используют МРТ для более детального изучения. МРТ обычно позволяет определить, является ли этот патологический участок опухолью, инфекцией или повреждением кости, вызванным другой причиной. МРТ для определения размеров опухоли: МРТ помогает врачам оценить степень распространения рака в организме (размеры опухоли). Этот вид визуализации показывает костный мозг внутри костей и мягкие ткани вокруг опухоли, включая расположенные рядом кровеносные сосуды и нервы. МРТ также может показать любые небольшие опухоли костей, расположенные на расстоянии нескольких сантиметров от основной опухоли, так называемые метастазы, распространяющиеся за пределы опухоли . Знание размеров опухоли очень важно при планировании операции.
Компьютерная томография (КТ) объединяет множество рентгеновских снимков для получения подробных поперечных изображений внутренних органов. Перед исследованием могут ввести внутривенно контрастное вещество для получения более четкого изображения.
- Если рентгенография костей выявляет опухоль, иногда для определения того, распространилась ли опухоль на близлежащие мышцы, жировую ткань или сухожилия, используется компьютерная томография, хотя МРТ для этой цели часто оказывается более подходящим методом.
- Компьютерная томография часто проводится для выявления возможного распространения рака в другие части тела, такие как легкие, печень или другие органы.
Биопсия иглой под контролем КТ: компьютерная томография (КТ) также может использоваться для направления биопсийной иглы в опухоль. Для этого исследования пациент остается на столе КТ-сканера, пока врач перемещает биопсийную иглу к опухоли. КТ-сканирование повторяется до тех пор, пока кончик иглы не окажется внутри образования.
Позитронно-эмиссионная томография (ПЭТ или ПЭТ-сканирование). ПЭТ-сканирование может помочь выявить распространение рака костей на легкие, другие кости или другие части тела. Этот вид визуализации может быть повторен во время лечения, чтобы оценить его эффективность.
Для проведения ПЭТ-сканирования в кровь вводят радиоактивный сахар. Количество радиоактивности очень мало, и он выводится из организма в течение суток или около того. Поскольку раковые клетки быстро растут, они поглощают большое количество сахара. Эти участки видны на ПЭТ-скане. Примерно через час после инъекции пациента перекладывают на стол в ПЭТ-сканере, на столе пациент лежит около 30 минут, пока специальная камера создает изображение областей радиоактивности в теле. Изображение не такое детализированное, как при КТ или МРТ, но оно предоставляет полезную информацию о вашем теле в целом. ПЭТ/КТ-сканирование: Некоторые аппараты позволяют проводить ПЭТ и КТ-сканирование одновременно (ПЭТ/КТ-сканирование). Это позволяет врачу сравнить области с повышенной радиоактивностью на ПЭТ-скане с более подробным изображением этой области на КТ-скане.
Сцинтиграфия костей. Сцинтиграфия костей может показать, распространился ли рак на другие кости. Она часто является частью обследования людей с раком костей. Этот тест полезен, поскольку позволяет увидеть весь скелет сразу. ПЭТ-сканирование, описанное выше, часто предоставляет аналогичную информацию, поэтому сцинтиграфия костей может не потребоваться, если проведут ПЭТ-сканирование. Для этого теста небольшое количество низкоактивного радиоактивного вещества, называемого технецием-99, вводится в кровь и достигает костей. Затем специальная камера, способная обнаруживать радиоактивность, создает изображение скелета. Области активных изменений костной ткани притягивают радиоактивность и выглядят как «горячие точки» на скелете. Горячие точки могут указывать на наличие раковых клеток, но аналогичные изменения могут наблюдаться и при других заболеваниях костей. Для постановки точного диагноза могут потребоваться дополнительные исследования, такие как рентгенография, МРТ или даже биопсия. В этом тесте используется очень низкая доза радиоактивности, и вещество выводится из организма в течение суток или около того.
Биопсия. Результаты диагностических исследований могут убедительно указывать на рак кости, но биопсия — единственный способ убедиться в этом наверняка. Во время биопсии врач берет один или несколько фрагментов опухоли для исследования. Если эти анализы покажут, что опухоль является раком кости, дополнительные лабораторные исследования образца биопсии помогут онкологической команде определить, как быстро опухоль может расти или распространяться, и какие методы лечения будут наиболее эффективны. Важно, чтобы биопсию кости проводил специалист по опухолям костей, иначе это может привести к проблемам в дальнейшем. По возможности, биопсию и хирургическое лечение следует планировать одновременно, и оба вмешательства должен проводить один и тот же врач. Правильное планирование биопсии может помочь предотвратить осложнения в будущем и уменьшить объем хирургического вмешательства, необходимого в дальнейшем. Иногда неправильно выполненная биопсия может затруднить последующее удаление всех раковых клеток хирургом, что может потребовать более обширного хирургического вмешательства. Это также может увеличить риск распространения рака.
Тип биопсии, который вам необходим, зависит от следующих факторов:
- Независимо от того, выглядит ли опухоль доброкачественной (не раковой) или злокачественной (раковой).
- Тип опухоли, который, скорее всего, диагностирован, определяется на основании результатов визуализационных исследований, возраста и локализации опухоли.
Некоторые виды опухолей костей можно диагностировать с помощью биопсии иглой. Другие типы опухолей костей требуют диагностики с помощью более крупного образца, полученного в ходе хирургической биопсии. Если онкологическая команда планирует удалить всю опухоль во время биопсии, это также повлияет на тип проводимой биопсии.
Пункционная биопсия. При этом виде биопсии тонкая полая игла вводится через кожу в опухоль для взятия небольшого образца. Обычно это делается под местной анестезией, когда обезболивающее средство вводится в кожу и другие ткани над местом биопсии. В этом случае пациент будет бодрствовать во время биопсии, но чувствовует минимальную боль или ее полное отсутствие. В некоторых ситуациях может потребоваться седация или введение в глубокий сон (общая анестезия). Если подозрительный участок находится близко к поверхности тела, врач часто может направить иглу, прощупав этот участок. Если опухоль не прощупывается, потому что находится слишком глубоко, врач может ввести иглу в опухоль с помощью методов визуализации, таких как ультразвуковое исследование или компьютерная томография.
Тонкоигольная аспирационная биопсия (ТАБ). Этот вид биопсии обычно не используется для диагностики опухоли кости. Однако его можно использовать для подтверждения распространения рака на кость (метастазы) или рецидива рака кости (рака, который возвращается после лечения).
Этот вид биопсии не позволяет увидеть структуру кости и часто позволяет получить очень небольшое количество клеток, слишком малое для диагностики новой опухоли.
Хирургическая биопсия. При таком виде биопсии врач (обычно ортопед) удаляет часть опухоли через разрез на коже.
- Инцизионная биопсия : удаляется только часть опухоли.
- Эксцизионная биопсия : удаляется вся опухоль.
Эти биопсии часто проводятся в операционной под общим наркозом (препаратом, погружающим пациента в глубокий сон). Также их можно проводить с использованием блокады нерва, которая обезболивает большую часть тела.
Вопросы, которые следует задать перед проведением биопсии кости.
- Какой у вас опыт проведения биопсии такого типа?
- Вы входите в состав команды, занимающейся лечением рака костей?
- Что будет происходить во время биопсии?
- Сколько времени потребуется для получения результатов?
Лабораторные исследования образцов биопсии. Патолог изучит образцы биопсии под микроскопом. Патолог — это врач, специализирующийся на определенных лабораторных исследованиях. Если он обнаружит раковые клетки, он также может провести анализы для выявления хромосомных или генетических изменений в опухолевых клетках. Эти тесты могут помочь диагностировать некоторые виды опухолей костей и предсказать, насколько хорошо рак может отреагировать на определенные виды лечения. Патолог также присвоит раку степень злокачественности. Это показатель того, насколько быстро он, вероятно, будет расти и распространяться, исходя из внешнего вида опухолевых клеток. Раковые образования, которые внешне напоминают нормальную костную ткань, описываются как низкозлокачественные и, как правило, растут медленнее. Раковые образования, которые выглядят очень аномально, называются высокозлокачественными.
Анализы крови. Анализы крови не являются обязательными для диагностики рака костей, но могут быть полезны после постановки диагноза.
Например, высокий уровень таких химических веществ в крови, как щелочная фосфатаза и лактатдегидрогеназа (ЛДГ), может указывать на более запущенную стадию рака. Однако эти показатели также могут быть повышены из-за других заболеваний, не связанных с раком.
- Общий анализ крови (ОАК) измеряет уровень лейкоцитов, эритроцитов и тромбоцитов в крови. Этот анализ может использоваться во время лечения, например, химиотерапии, для выявления возможных проблем или побочных эффектов.
- Биохимический анализ крови позволяет оценить работу печени и почек, а также уровень определенных минералов в крови. Часто это проверяется перед операцией или химиотерапией.
- Для проверки способности крови к нормальному свертыванию можно провести коагуляционный тест , что особенно важно перед операцией.
Стадии рака костей
Если был диагностирован рак костей, онкологическая команда попытается выяснить, распространился ли он, и если да, то насколько. Этот процесс называется стадированием. Стадия рака описывает, насколько распространена опухоль в организме. Она помогает определить, насколько серьезна болезнь и как лучше всего ее лечить.
Стадия рака костей определяется на основании результатов таких исследований, как физический осмотр, визуальные методы и биопсия.
Система стадирования — это стандартный способ, используемый командой специалистов по лечению рака для оценки степени распространения заболевания. Для рака костей используется несколько систем стадирования.
В некоторых случаях рак костей описывают с помощью таких терминов, как:
- Локализованные (одна единственная опухоль) или метастатические (опухоли, распространившиеся по всему организму)
- Низкосортный или высокосортный
Случай рака также может быть описан с использованием числовой системы:
- Система MSTS использует номера I (1) – III (3)
- Система AJCC использует числа I (1) – IV (4)
Эти две системы описаны более подробно ниже.
Система стадирования Общества по изучению опухолей опорно-двигательного аппарата (MSTS)
Одной из систем, используемых для определения стадии рака костей, является система MSTS , также известная как система Эннекинга. Она основана на трех ключевых элементах информации:
Степень злокачественности рака (G)
Степень злокачественности (G) рака — это показатель вероятности его роста и распространения. В этой системе раковые заболевания делятся на низкозлокачественные (G1) и высокозлокачественные (G2) в зависимости от того, как выглядят клетки под микроскопом.
- Низкая степень злокачественности (G1): раковые клетки больше похожи на нормальные клетки и с меньшей вероятностью быстро растут и распространяются.
- Высокая степень злокачественности (G2): раковые клетки выглядят более аномальными.
Размер первичной опухоли (Т)
Размеры первичной опухоли (Т) классифицируются следующим образом:
- Внутрикомпартментальный (Т1) : опухоль в основном осталась в пределах кости.
- Экстракомпартментальный (Т2) : опухоль распространилась за пределы кости в другие близлежащие структуры.
Метастазы (М)
Если опухоль метастазировала (М), это означает, что она распространилась на другие области. Это могут быть близлежащие лимфатические узлы (скопления клеток иммунной системы размером с фасоль) или другие органы.
- M0: опухоль не распространилась на лимфатические узлы или другие органы (локализованная).
- Опухоль распространилась на лимфатические узлы или другие органы (метастатический эффект).
Общий этап
Эти факторы объединяются для определения общей стадии, используя числа от I (1) до III (3). Стадии I и II делятся на A для внутрикомпартментальных опухолей и B для внекомпартментальных опухолей.
- Стадия IA или IB: низкозлокачественные локализованные опухоли
- Стадия IIA или IIB: Высокозлокачественные локализованные опухоли
- III стадия: Метастатические опухоли, независимо от степени злокачественности.
Система стадирования AJCC TNM
Еще одна система стадирования, иногда используемая для рака костей, — это система TNM Американского объединенного комитета по раку (AJCC) . Эта система основана на 4 ключевых элементах информации:
- Размер первичной опухоли (Т) описывает размер основной (первичной) опухоли и наличие у нее очагов в нескольких местах в костях.
- Распространение в лимфатические узлы (N) описывает степень распространения на близлежащие (региональные) лимфатические узлы. Опухоли костей редко распространяются на лимфатические узлы.
- Метастазы (М) указывают на то, что рак метастазировал (распространился) на другие органы тела. Чаще всего метастазы поражают легкие или другие кости.
- Степень злокачественности (G) обозначает степень развития опухоли. Под микроскопом клетки опухоли низкой степени злокачественности больше похожи на нормальные клетки и с меньшей вероятностью быстро растут и распространяются. Клетки опухоли высокой степени злокачественности выглядят более аномально.
Цифры или буквы: Цифры или буквы после T, N, M и G предоставляют более подробную информацию о каждом из этих факторов. Более высокие числа, как правило, означают, что рак имеет более тревожные признаки.
Общая стадия: После определения категорий T, N и M и степени злокачественности рака кости информация объединяется в общую стадию. Эти стадии отличаются от системы MSTS. Они описываются числами от I (1) до IV (4) и иногда подразделяются на более мелкие.
Этап I
Этап IA
- Основная опухоль имеет диаметр не более 8 сантиметров* (Т1).
- Рак не распространился на близлежащие лимфатические узлы (N0).
- Рак не распространился на отдаленные части тела (M0).
- Рак относится к низкой степени злокачественности (G1) или степень злокачественности определить невозможно (GX).
*8 сантиметров = примерно 3 дюйма
Этап IB
- Основная опухоль имеет диаметр более 8 сантиметров (T2) или в одной кости находится более одной опухоли (T3).
- Рак не распространился на близлежащие лимфатические узлы (N0).
- Рак не распространился на отдаленные части тела (M0).
- Рак относится к низкой степени злокачественности (G1) или степень злокачественности определить невозможно (GX).
Этап II
Этап IIA
- Основная опухоль имеет диаметр не более 8 сантиметров* (Т1).
- Рак не распространился на близлежащие лимфатические узлы (N0).
- Рак не распространился на отдаленные части тела (M0).
- Рак относится к высокой степени злокачественности (G2 или G3).
*8 сантиметров = примерно 3 дюйма
Этап IIB
- Основная опухоль имеет диаметр более 8 сантиметров (Т2).
- Рак не распространился на близлежащие лимфатические узлы (N0).
- Рак не распространился на отдаленные части тела (M0).
- Рак относится к высокой степени злокачественности (G2 или G3).
Этап III
- В одной и той же кости (Т3) обнаруживается более одной опухоли.
- Рак не распространился на близлежащие лимфатические узлы (N0).
- Рак не распространился на отдаленные части тела (M0).
- Рак относится к высокой степени злокачественности (G2 или G3).
IV стадия
Стадия IVA
- Основная опухоль может быть любого размера, и в кости (любой Т‑образной) может быть более одной опухоли.
- Рак не распространился на близлежащие лимфатические узлы (N0).
- Заболевание распространилось только на легкие (M1a).
- Это может быть любая оценка (любая G).
Стадия IVB
- Основная опухоль может быть любого размера, и в кости (любой Т‑образной) может быть более одной опухоли.
- Рак распространился на близлежащие лимфатические узлы (N1).
- Вирус мог распространиться на отдаленные органы, такие как легкие или другие кости (любая форма).
- Это может быть любая оценка (любая G).
ИЛИ
- Основная опухоль может быть любого размера, и в кости (любой Т‑образной) может быть более одной опухоли.
- Рак мог распространиться на близлежащие лимфатические узлы (любые N), а мог и не распространиться.
- Оно распространилось на отдаленные части тела, такие как другие кости, печень или мозг (M1b).
- Это может быть любая оценка (любая G).
Определение стадии заболевания может быть сложным и запутанным процессом.
Лечение рака костей
Лечение рака костей у взрослых зависит от типа рака костей, его локализации, стадии (степени распространения), общего состояния здоровья и предпочтений пациента, а также других факторов.
Основные методы лечения рака костей:
- Операция
- Лучевая терапия
- Химиотерапия
- Таргетная и иммунотерапия
Часто используется несколько видов лечения. Лечение этих видов рака может быть сложным, поэтому зачастую оптимальным является лечение командой врачей разных специальностей, имеющих опыт работы с ними.
Хирургическое лечение рака костей
Хирургическое вмешательство является важной частью лечения большинства видов рака костей. Обычно оно включает в себя:
- Биопсия для диагностики рака.
- Хирургическое удаление опухоли (опухолей).
Биопсия и хирургическое удаление опухоли
По возможности крайне важно, чтобы биопсия для диагностики рака кости планировалась одновременно с операцией по удалению опухоли.
Также очень важно, чтобы биопсию и операцию проводил опытный хирург-ортопед. Биопсия должна быть выполнена определенным образом. Это дает наилучшие шансы на сокращение объема необходимой операции в будущем.
Главная цель операции — удалить всю раковую опухоль. Если останется даже небольшое количество раковых клеток, они могут разрастись и образовать новую опухоль или распространиться на другие части тела. Чтобы снизить риск этого, хирурги удаляют опухоль вместе с частью окружающей здоровой ткани. Это называется широким иссечением .
Чего ожидать от операции?
Тип хирургического вмешательства будет зависеть главным образом от расположения и размера опухоли. Все операции по удалению рака костей сложны, но опухоли в руках или ногах, как правило, удалять не так сложно, как опухоли в челюстной кости, у основания черепа, в позвоночнике или в тазовой кости.
Перед операцией хирург и анестезиолог должны обсудить преимущества и риски планируемой операции. Краткосрочные осложнения после операции могут включать реакции на анестезию, кровотечение, образование тромбов, боль и инфекции. Долгосрочные осложнения будут зависеть от конкретной операции.
Лабораторные анализы после операции
После операции врач, называемый патологоанатомом, изучит удаленную ткань, чтобы определить, есть ли раковые клетки по краям (наружным кромкам).
- Положительные края резекции: если раковые клетки обнаруживаются по краям ткани, края считаются положительными. Положительные края резекции могут означать, что часть раковых клеток осталась в ткани.
- Отрицательные края: если по краям ткани не обнаружено раковых клеток, говорят, что края чистые, без раковых клеток. Широкое иссечение с чистыми краями помогает снизить риск рецидива рака.
Хирургическое лечение опухолей костей в руках или ногах.
Опухоли в руках или ногах могут лечиться одним из следующих способов:
- Хирургическое вмешательство с сохранением конечности: удаление раковой опухоли и части окружающих здоровых тканей, но с сохранением конечности в основном неповрежденной.
- Ампутация: удаление раковой опухоли и всей или части руки или ноги.
Пластическая хирургия с сохранением конечности. В большинстве случаев пациентам с опухолями в руках или ногах возможна органосохраняющая операция, но это зависит от расположения опухоли, ее размера и от того, распространилась ли она на соседние структуры.
Сохранить конечность — очень сложная операция. Хирурги, выполняющие её, должны обладать специальными навыками и опытом. Задача состоит в том, чтобы удалить всю опухоль, сохранив при этом близлежащие сухожилия, нервы и кровеносные сосуды, чтобы максимально сохранить функцию и внешний вид конечности. Если рак распространился на эти структуры, их необходимо удалить вместе с опухолью. В таких случаях ампутация иногда является наилучшим вариантом.
Костный трансплантат или внутренний протез. Хирург также должен восстановить удаленный участок кости вместе с опухолью. Этот участок кости заменяется одним из следующих материалов:
- Костная трансплантация: фрагмент кости из другой части вашего тела или от другого человека.
- Внутренний протез: устройство, изготовленное из металла и других материалов, которое заменяет часть или всю кость.
В некоторых случаях используются как трансплантат, так и протез.
Возможные осложнения. Осложнения органосохраняющей хирургии могут включать инфекции, а также расшатывание или поломку трансплантатов или стержней. Пациентам, перенесшим органосохраняющую операцию, в последующие годы может потребоваться еще одна операция. Некоторым в конечном итоге может потребоваться ампутация.
Ампутация. Для некоторых людей ампутация может быть наилучшим вариантом. Например, если опухоль очень большая или если она распространяется на нервы и/или кровеносные сосуды, сохранить конечность может быть невозможно. Некоторые люди выбирают ампутацию, даже когда возможно сохранение конечности, по причинам, которые часто включают ограничения в физической активности.
Планирование перед ампутацией. Хирург определяет, какую часть руки или ноги необходимо ампутировать, на основании результатов МРТ-сканирования и заключения патологоанатома о ткани, удаленной во время операции. Операция обычно планируется таким образом, чтобы мышцы и кожа образовали манжету вокруг оставшейся кости. Эта манжета будет крепиться к концу протеза (искусственной конечности). Другой вариант — имплантация протеза в оставшуюся кость, при этом конец протеза будет оставаться снаружи кожи. Затем его можно будет прикрепить к внешнему протезу.
Реконструктивная хирургия. Реконструктивная хирургия может помочь некоторым людям, потерявшим конечность, восстановить максимально возможную функциональность.
Например, если ногу необходимо ампутировать посередине бедра, включая коленный сустав, голень и стопу можно повернуть и прикрепить к бедренной кости так, чтобы голеностопный сустав функционировал как новый коленный сустав. Эта операция называется ротационной пластикой . После такой операции все равно понадобится протез для замены нижней части ноги. При правильной физиотерапии человек часто может ходить самостоятельно через 3–6 месяцев после ампутации ноги.
Если опухоль находится в плече или верхней части руки и требуется ампутация, в некоторых случаях можно удалить область с опухолью и пришить нижнюю часть руки обратно, так что человек получит функциональную, но значительно укороченную руку.
Реабилитация после операции. Это может быть самой сложной частью лечения, и здесь невозможно описать её полностью. Перед операцией может быть полезно встретиться со специалистом по реабилитации, чтобы узнать о доступных вариантах и о том, что может потребоваться после операции.
Реабилитация после ампутации обычно занимает меньше времени, чем реабилитация после органосохраняющей операции. Например, если опухоль находится на кости ноги:
- После ампутации ноги люди часто начинают ходить через 3–6 месяцев.
- После операции по сохранению конечности в среднем требуется около года, чтобы люди заново научились ходить.
Физическая реабилитация после операции по сохранению конечности также намного интенсивнее, чем после ампутации, но она все равно чрезвычайно важна. Очень важно, чтобы вы активно участвовали в программе реабилитации после операции. Активное участие даст вам наилучшие шансы сохранить функции сохраненной руки или ноги, чтобы в дальнейшем не пришлось ее ампутировать.
Хирургическое лечение опухолей костей в других частях тела.
Тазовые (бедренные) кости. Опухоли в тазовых (бедренных) костях часто трудно полностью удалить хирургическим путем. Некоторые виды опухолей можно сначала лечить химиотерапией , чтобы уменьшить размер опухоли и облегчить операцию. В некоторых случаях после операции можно восстановить тазовые кости, но в ряде случаев может потребоваться удаление тазовых костей и ноги, к которой они прикреплены.
Нижняя челюсть. При опухолях нижней челюсти может быть удалена вся нижняя половина челюсти, а затем заменена костью из других частей тела. Если хирургу не удается удалить всю опухоль, может быть применена лучевая терапия .
Позвоночник или череп. При опухолях в таких областях, как позвоночник или череп, безопасное удаление всей опухоли может быть невозможно. Раковые заболевания в этих костях могут потребовать комбинированного лечения.
Суставы. При опухолях, поражающих суставы, после удаления опухоли может оказаться невозможным восстановление сустава. В этом случае может потребоваться артродез (сращение сустава). Это хирургическая операция по соединению двух костей. Чаще всего она применяется при опухолях позвоночника, но может использоваться и в других частях тела, например, в плечевом или тазобедренном суставе.
Кюретаж (внутриочаговое иссечение). Некоторые виды опухолей костей менее склонны к распространению или рецидиву после лечения. В этом случае хирург может удалить опухоль, не удаляя часть кости.
Эта процедура называется кюретажем (внутриочаговым иссечением) . Она выполняется острым инструментом, называемым кюреткой, и оставляет отверстие в кости. После удаления максимально возможной части опухоли хирург может обработать близлежащую костную ткань другими методами, такими как химические вещества или сильный холод (криохирургия), чтобы попытаться уничтожить оставшиеся опухолевые клетки.
Костный цемент. После кюретажа можно заполнить образовавшееся отверстие костным цементом и укрепить оставшуюся кость. Костный цемент ПММА (полиметилметакрилат) изначально находится в жидком состоянии и со временем затвердевает. Его можно ввести в отверстие в кости в жидком виде после кюретажа. При затвердении он выделяет много тепла, что может помочь уничтожить оставшиеся опухолевые клетки.
Хирургическое лечение метастазов опухолей костей.
Если рак костей распространился (метастазировал) на другие части тела, эти опухоли необходимо удалить, чтобы иметь шанс на излечение.
Рак костей, распространившийся на легкие. При распространении рака костей чаще всего поражаются легкие. Если возможно хирургическое удаление этих метастазов, его необходимо тщательно спланировать. Перед операцией хирург учтет, находятся ли опухоли в одном или обоих легких, общее количество опухолей, их размер, а также общее состояние здоровья пациента.
Диагностические исследования, такие как компьютерная томография грудной клетки, могут не показать все опухоли, поэтому хирург должен подготовить план лечения на случай, если во время операции будут обнаружены дополнительные опухоли.
Рак костей, распространившийся на другие кости или органы. Некоторые виды рака костей могут распространяться на другие кости или на такие органы, как почки, печень или мозг. Возможность хирургического удаления таких опухолей зависит от их размера, расположения и других факторов.
Когда хирургическое лечение метастазов невозможно.Не все метастатические раковые заболевания можно удалить хирургическим путем. Некоторые метастазы могут быть слишком большими или расположены слишком близко к важным структурам, таким как крупные кровеносные сосуды, чтобы их можно было безопасно удалить. Люди с другими серьезными проблемами со здоровьем, такими как заболевания сердца, печени или почек, могут не выдержать стресса, связанного с анестезией и хирургическим вмешательством по удалению метастазов.
В этом случае могут быть предложены другие методы лечения, чтобы попытаться контролировать эти опухоли как можно дольше.
Лучевая терапия при раке костей
Лучевая терапия использует высокоэнергетические лучи или частицы для уничтожения раковых клеток. Это способ уничтожения раковых клеток, которые невозможно удалить хирургическим путем. Лучевая терапия нечасто играет важную роль в лечении рака костей, но может применяться в некоторых случаях.
Клетки рака костей нелегко уничтожить с помощью радиации, поэтому она редко играет важную роль в лечении этих видов рака.
Лучевая терапия может применяться в некоторых ситуациях.
- После операции: если неясно, что вся опухоль была удалена. Например, может быть применена лучевая терапия, если раковые клетки были обнаружены по краям (границам) удаленной ткани. Это делается для того, чтобы попытаться уничтожить любые оставшиеся раковые клетки.
- Вместо хирургического вмешательства: если рак кости невозможно полностью удалить (резецировать), лучевая терапия может замедлить рост опухоли и контролировать такие симптомы, как боль и отек. Это может проводиться в сочетании с другими методами лечения.
- Если рак вернется: лечите симптомы и замедляйте повторный рост раковых клеток.
Как это проводится?
Этот вид лечения проводится врачом, которого называют радиоонкологом.
Моделирование лечения: Перед началом лечения врач лучевой терапии составляет план лечения. Во время сеанса, называемого моделированием лечения, они используют такие исследования, как МРТ, для проведения точных измерений. На основе этих исследований и типа рака определяется доза облучения и место его применения. Область, куда направляется облучение, называется полем облучения.
Изготовление слепка или гипсовой повязки: Важно, чтобы облучение проводилось точно в том поле, которое было запланировано в симуляции могут изготовить пластиковый слепок, похожий на гипсовую повязку, чтобы удерживать пациента в одном и том же положении во время каждого сеанса лечения.
Во время лечения: лучевая терапия обычно проводится пять дней в неделю в течение нескольких недель. Этот вид лечения похож на рентгеновское обследование, хотя доза облучения значительно выше. Во время каждого сеанса пациент лежит на специальном столе, а аппарат проводит облучение. Процедуры безболезненны. Каждый сеанс длится от 15 до 30 минут. Большая часть этого времени уходит на то, чтобы убедиться в правильном направлении излучения.
Какой вид лучевой терапии используется при раке костей?
Современные методы позволяют врачам направлять лучевую терапию на опухоли с большей точностью, чем это было возможно раньше. Оптимальный подход к лучевой терапии может быть индивидуальным для каждого пациента и зависит от типа опухоли кости, а также от квалификации специалистов и оборудования, имеющихся в лечебном центре.
Лучевая терапия с модуляцией интенсивности (IMRT). IMRT — это усовершенствованная форма трехмерной лучевой терапии. Помимо формирования пучков и их направления на опухоль под разными углами, интенсивность (сила) пучков регулируется для ограничения дозы, достигающей наиболее чувствительных здоровых тканей. Это позволяет врачам доставлять более высокую дозу в области опухоли. Многие крупные больницы и онкологические центры в настоящее время используют IMRT.
Протонная лучевая терапия. Протонный пучок использует радиоактивные частицы, которые проходят лишь определенное расстояние, прежде чем высвободить большую часть своей энергии. Этот вид лечения может быть полезен при лечении опухолей в небольших, труднодоступных местах, таких как основание черепа или позвоночник, где очень важно ограничить воздействие радиации на близлежащие здоровые ткани.
Терапия ионами углерода. Подобно протонной лучевой терапии, этот метод ограничивает воздействие радиации на здоровые ткани и фокусирует энергию излучения на опухоли. Этот метод доступен лишь в немногих центрах мира.
Стереотактическая радиохирургия (СРС). Этот метод позволяет врачам доставлять большую дозу радиации на небольшой участок опухоли, обычно за один сеанс. После проведения диагностических исследований, позволяющих точно определить местоположение опухоли, на эту область направляется очень тонкий пучок излучения под разными углами. Обычно это делается с помощью источника излучения на конце роботизированной руки, управляемой компьютером, которая вращается вокруг пациента, лежащего на столе. Иногда врачи проводят лучевую терапию в несколько этапов, чтобы доставить одинаковую дозу или немного большую. Это называется стереотактической лучевой терапией тела (SBRT) .
Побочные эффекты лучевой терапии
Побочные эффекты лучевой терапии зависят от дозы облучения и места его проведения. Кратковременные побочные эффекты возникают во время или вскоре после лечения. Долгосрочные побочные эффекты могут проявиться через несколько месяцев или лет.
Кратковременные побочные эффекты. В течение нескольких недель во время и после лечения могут наблюдаться следующие побочные эффекты:
- Усталость
- Выпадение волос в области, подвергающейся облучению.
- Покраснение, болезненность или сухость кожи в области облучения, как при солнечном ожоге.
- Низкий уровень клеток крови (это чаще встречается при сочетании лучевой терапии с химиотерапией или другими препаратами).
- Язвы во рту, затруднение глотания или потеря аппетита вследствие облучения области головы и шеи.
- Тошнота, рвота, спазмы и/или диарея вследствие облучения брюшной полости или таза.
- Повреждение мочевого пузыря, которое может вызывать боль или проблемы при мочеиспускании (в результате облучения брюшной полости или таза).
Долгосрочные побочные эффекты. Радиация влияет на то, как кости и ткани восстанавливаются после повреждений, растут и функционируют. Многие отдаленные последствия радиации зависят от места облучения.
Например:
- При облучении руки или ноги рубцы после лучевой терапии могут привести к ограничению движений, требующему лечения.
- Облучение шеи или челюсти может повлиять на состояние челюсти или зубов.
- Облучение области таза может повлиять на выработку половых гормонов яичками или яичниками.
Риск развития вторичного рака
Поскольку радиация разрушает ДНК, она также может увеличить риск развития вторичного рака спустя много лет. В зависимости от места облучения может быть рекомендовано раннее обследование на рак.
Контрольные визиты после лучевой терапии. Чтобы снизить риск серьезных долгосрочных последствий лучевой терапии, врачи стараются использовать минимально возможную дозу облучения. Тем не менее, важно регулярно посещать врача для контрольных осмотров, чтобы в случае возникновения проблем их можно было выявить и вылечить как можно скорее.
Химиотерапия при раке костей
Химиотерапия часто является важной частью лечения саркомы Юинга, остеосаркомы и недифференцированной плеоморфной саркомы (НПС).
Этот метод не так часто используется при большинстве других типов рака костей, таких как гигантоклеточные опухоли и большинство типов хордом и хондросарком. Эти виды рака не очень чувствительны к химиотерапии, поэтому сначала могут быть опробованы другие препараты.
Химиотерапия — это применение лекарственных препаратов для лечения рака. Эти препараты обычно вводятся внутривенно и могут достигать раковых клеток и уничтожать их в любой части тела.
Какие химиотерапевтические препараты используются для лечения рака костей?
К числу химиотерапевтических препаратов, используемых для лечения рака костей, относятся:
- Доксорубицин (Адриамицин)
- Цисплатин
- Этопозид (ВП-16)
- Ифосфамид
- Циклофосфамид
- Метотрексат
- Винкристин
- Дактиномицин
- Топотекан
- Иринотекан
- Темозоломид
- Лурбинектидин
- Карбоплатин
- Гемцитабин
- Доцетаксел
В большинстве случаев назначают два или более препаратов одновременно. К распространенным комбинациям относятся:
Схема MAP: высокие дозы метотрексата, доксорубицина и цисплатина, иногда с ифосфамидом и/или этопозидом (MAPIE). Чаще всего используется для лечения остеосарком и недифференцированных плеоморфных сарком кости (UPS).
Схема лечения VDC/IE: винкристин, доксорубицин, циклофосфамид, ифосфамид и этопозид. Эта комбинация чаще всего используется для лечения саркомы Юинга.
Возможные побочные эффекты химиотерапии
Химиотерапевтические препараты воздействуют на быстрорастущие клетки. Раковые клетки быстро размножаются, но так же быстро размножаются и другие здоровые клетки организма, включая клетки крови, клетки волос и клетки слизистой оболочки кишечника. Когда химиотерапия повреждает эти быстрорастущие здоровые клетки, это может привести к побочным эффектам.
Эти побочные эффекты различаются в зависимости от типа химиотерапевтических препаратов, дозы и продолжительности их применения. Онкологическая команда будет внимательно следить за пациентами на предмет побочных эффектов.
Распространенные краткосрочные побочные эффекты. К числу распространенных краткосрочных побочных эффектов химиотерапии относятся:
- Тошнота и рвота
- Потеря аппетита
- Диарея или запор
- Выпадение волос
- Язвы во рту
Химиотерапия может повредить костный мозг, где образуются новые клетки крови. Это может снизить количество клеток крови, что приводит к следующим последствиям:
- Повышенная вероятность инфицирования (из-за недостатка лейкоцитов).
- Легкое кровотечение или образование синяков (из-за низкого уровня тромбоцитов)
- Усталость или одышка (из-за низкого уровня эритроцитов).
Контроль краткосрочных побочных эффектов. Для снижения риска серьезных инфекций иногда вместе с химиотерапией назначают препараты, называемые факторами роста (например, филграстим, также известный как G‑CSF), чтобы помочь организму как можно быстрее вырабатывать новые белые кровяные клетки.
Большинство кратковременных побочных эффектов химиотерапии исчезают после завершения лечения. Часто существуют способы смягчить эти побочные эффекты во время лечения.
Например, вы можете принимать лекарства, которые помогут предотвратить и уменьшить тошноту и рвоту, или которые помогут нормализовать показатели крови.
Долгосрочные побочные эффекты. Химиотерапия также может иметь некоторые долгосрочные побочные эффекты. Например, некоторые лекарства могут повышать риск развития в будущем другого типа рака, такого как лейкемия. Этот риск серьезен, но встречается нечасто. Небольшое повышение риска необходимо сопоставить с важностью химиотерапии при лечении рака костей.
Таргетная терапия и иммунотерапия при раке костей
В последние годы исследователи разработали нехимиотерапевтические препараты, которые можно использовать в рамках лечения некоторых видов рака костей. Эти препараты действуют иначе, чем стандартные химиотерапевтические средства, и, как правило, имеют другие побочные эффекты.
- Таргетная терапия: Некоторые препараты таргетной терапии целенаправленно воздействуют на изменения генов внутри клеток, которые могут привести к раку костей. Таргетные препараты особенно важны при лечении тех типов рака костей, при которых химиотерапия оказалась неэффективной, например, хордом.
- Иммунотерапия: Препараты для иммунотерапии также используются в рамках лечения некоторых видов рака костей. Иммунотерапия — это применение лекарственных средств, помогающих иммунной системе распознавать и уничтожать раковые клетки.
Остеосаркома: таргетная терапия. Для лечения некоторых видов остеосаркомы используется класс препаратов, называемых ингибиторами тирозин-киназы (ИТК).
Хондросаркома: таргетная терапия. Препараты таргетной терапии являются частью лечения некоторых видов хондросаркомы. Эти препараты могут применяться в определенных ситуациях, например:
- Когда в опухоли присутствуют специфические изменения генов
- Если рак распространился по всему организму.
Для лечения хондросаркомы иногда используются иммунотерапевтические препараты, называемые ингибиторами иммунных контрольных точек .
Ингибиторы иммунных контрольных точек
Важная часть иммунной системы — это её способность предотвращать атаку на нормальные клетки организма. Для этого она использует «контрольные» белки на иммунных клетках. Они действуют как переключатели, которые необходимо включить или выключить, чтобы запустить иммунный ответ. Раковые клетки иногда используют эти контрольные точки, чтобы избежать атаки со стороны иммунных клеток.
Препараты, воздействующие на эти контрольные точки, называемые ингибиторами контрольных точек , могут использоваться для лечения некоторых пациентов с хондросаркомой. К ним относятся:
- Пембролизумаб (Кейтруда)
- Ниволумаб (Опдиво)
Эти препараты вводятся внутривенно (в/в) один раз в несколько недель. Пембролизумаб также доступен в виде инъекций.
Распространенные побочные эффекты
К распространенным побочным эффектам этих препаратов относятся усталость, кашель, кожная сыпь, потеря аппетита, запор, боли в суставах и диарея.
Серьезные побочные эффекты
В некоторых случаях при приеме этих препаратов могут возникать серьезные побочные эффекты. Эти проблемы могут быть серьезными и даже угрожающими жизни.
- Во время внутривенного введения этих препаратов может возникнуть инфузионная реакция. Симптомы могут включать лихорадку, озноб, сыпь, головокружение, свистящее дыхание и затрудненное дыхание.
- Эти препараты также могут вызывать атаку иммунных клеток на нормальные здоровые клетки по всему организму, что приводит к проблемам с легкими, кишечником, железами, вырабатывающими гормоны, такими как щитовидная железа, почками или другими органами.
Саркомы Юинга и саркомы, подобные саркоме Юинга: таргетная терапия. Препараты таргетной терапии являются частью лечения некоторых сарком Юинга и сарком, подобных саркоме Юинга. Эти препараты могут применяться в определенных ситуациях, например, при распространении заболевания по всему организму или при рецидиве рака после лечения.
более серьезным побочным эффектам относятся проблемы с кровоснабжением сердца, кровотечения, отклонения в результатах анализов щитовидной железы и перфорации (отверстия) в желудке или кишечнике.
Недифференцированная плеоморфная саркома (НПС): таргетная терапия. Лечение УПС аналогично лечению остеосаркомы. Для лечения некоторых из этих опухолей используются препараты класса ингибиторов тирозин-киназы (ИТК). Эти препараты могут применяться, если рак распространился на другие части тела или если рак рецидивирует после лечения.
Фибросаркома кости: таргетная терапия. В настоящее время таргетные препараты не используются для лечения фибросаркомы кости. Если существует препарат, воздействующий на изменение гена в клетках опухоли, ваша онкологическая команда может попробовать эти методы лечения. Но это обычно происходит только после таких методов лечения, как хирургическое вмешательство и лучевая терапия, которые, как известно, эффективны при таких типах опухолей.
Гигантоклеточные опухоли костей: таргетная терапия. Деносумаб (Xgeva) — это моноклональное антитело, блокирующее RANKL, белок, активирующий остеокласты, тип клеток, резорбирующих костную ткань. Это блокирует рост опухоли при гигантоклеточных опухолях кости.
Этот препарат вводят инъекционно один раз в несколько недель. К побочным эффектам этого препарата могут относиться усталость, слабость, тошнота и диарея.
К менее распространенным, но серьезным побочным эффектам относятся проблемы с челюстной костью (остеонекроз) или перелом кости в ноге. У людей, принимающих этот препарат, также может наблюдаться низкий уровень кальция, и они подвержены более высокому риску инфекций.
Хордомы: таргетная терапия. Ингибиторы тирозин-киназы действуют, блокируя сигналы, необходимые клеткам для роста и деления. Некоторые ингибиторы тирозинкиназы, такие как лапатиниб , воздействуют на тип тирозинкиназы, называемый EGFR, что делает препарат более эффективным для опухолей со специфическими генными мутациями. Другие ингибиторы тирозинкиназы блокируют сигналы от нескольких тирозинкиназ.
В качестве примеров ингибиторов тирозинкиназы, которые применялись при хордомах, можно привести следующие:
- Иматиниб (Гливек, Имкельди)
- Дазатиниб (Спрайсел)
- Сунитиниб (Сутент)
- Эрлотиниб (Тарцева)
- Лапатиниб (Тайкерб)
- Сорафениб (Нексавар)
Большинство этих препаратов принимаются внутрь в виде таблеток один или два раза в день. Иматиниб также выпускается в жидкой форме.
Побочные эффекты этих препаратов могут включать усталость, снижение количества клеток крови, потерю аппетита, синдром «рука-нога» (покраснение и раздражение рук и ног), высокое кровяное давление, потерю веса, диарею и боли в животе.
К менее распространенным, но более серьезным побочным эффектам относятся проблемы с кровоснабжением сердца, кровотечения, отклонения в результатах анализов щитовидной железы и перфорации (отверстия) в желудке или кишечнике.
Кто лечит рак костей?
При обнаружении опухоли кости важно, чтобы лечение проводилось опытной командой врачей.
Первичные опухоли костей встречаются редко, и их лечение может быть сложным. Рекомендуется командный подход, обычно в крупном онкологическом центре. В состав вашей лечебной команды могут входить следующие врачи:
- Хирург-ортопед : хирург, специализирующийся на мышцах и костях. Хирург-ортопед в составе онкологической бригады должен иметь опыт лечения опухолей костей.
- Онколог : врач, который лечит рак с помощью химиотерапии и других лекарственных препаратов.
- Радиационный онколог : врач, который лечит рак с помощью лучевой терапии.
- Врач-реабилитолог : врач, специализирующийся на реабилитации и физиотерапии.
В лечении могут участвовать и другие медицинские специалисты, в том числе помощники врачей, медицинские сестры, психологи, социальные работники, специалисты по реабилитации и другие медицинские работники.
Также очень важно задавать вопросы, если вы в чем-то не уверены.
Вопросы, которые следует задать перед началом лечения рака костей.
- Какие у меня есть варианты лечения?
- Что вы порекомендуете и почему?
- Какой у вас опыт лечения моего типа рака?
- Какие клинические исследования нам следует рассмотреть? Как мы можем узнать о них больше?
- Какова цель лечения?
- Каковы шансы рецидива рака при таком плане лечения?
- Стоит ли мне обратиться за вторым мнением? Как это сделать?
- Как скоро мне нужно начать лечение?
- Какие у меня будут варианты, если лечение не поможет и опухоль вернется?
Чего ожидать во время лечения
- Что мне нужно сделать, чтобы быть готовым к лечению?
- Сколько времени продлится лечение? Каким оно будет?
- Как мы узнаем, что лечение эффективно?
- Лечение будет проводиться в больнице, клинике или на дому?
- Могу ли я посещать работу или учебу во время лечения? Как лечение повлияет на мою повседневную жизнь?
Побочные эффекты и долгосрочные последствия
- Какие риски или побочные эффекты связаны с этими методами лечения?
- Какие побочные эффекты проявляются вскоре после лечения, а какие могут развиться позже?
- Можно ли что-нибудь сделать, чтобы справиться с побочными эффектами или избежать их?
- О каких симптомах или побочных эффектах мне следует сообщить вам немедленно?
- Как с вами можно связаться по вечерам, в праздничные дни или выходные?
Поддержка и ресурсы
- К кому я могу обратиться, если у меня возникнут вопросы о стоимости, страховом покрытии или социальной поддержке?
- Какое последующее наблюдение мне потребуется после лечения?
- Вы знаете какие-нибудь местные или онлайн-группы поддержки, где я мог бы поговорить с другими людьми, которые прошли через это?
После лечения рака костей
Рак костей и его лечение могут оказать глубокое влияние на восприятие себя и своего тела. Это также может повлиять на выполнение некоторых повседневных задач. Эти последствия часто наиболее выражены в течение первого года лечения, но у некоторых людей они могут быть длительными.
Отказ от лечения рака
Некоторые люди могут вообще не хотеть лечиться, особенно если рак находится в запущенной стадии. Причин для отказа от лечения может быть много, но важно обсудить это решение с вашей онкологической командой. Помните, что даже если вы решите не лечить рак, вы все равно можете получить поддерживающую терапию для облегчения боли или других симптомов.
паллиативная помощь
Людям с запущенным раком, которым, по прогнозам, осталось жить менее 6 месяцев, может быть полезно рассмотреть возможность получения паллиативной помощи. Паллиативная помощь призвана обеспечить наилучшее качество жизни людям, находящимся на заключительном этапе жизни.
Вам и вашей семье рекомендуется обсудить с вашей командой специалистов по лечению рака варианты паллиативной помощи, которые включают паллиативную помощь на дому, в специализированном хосписе или в других медицинских учреждениях.
Медицинский уход и специальное оборудование могут сделать пребывание дома приемлемым вариантом для многих семей.
